L'horreur de l'adsorption des échantillons sur les conteneurs (Partie 1)
Technical Advisor, Analytical & Measuring Instruments Division,
Shimadzu Corporation
Il y a eu des avancées étonnantes dans le développement des systèmes LC/MS et la technologie de séparation ces dernières années, ainsi que l'utilisation de plus en plus répandue de la LC/MS comme outil analytique attrayant pour diverses applications, y compris l'élucidation des phénomènes vitaux, le diagnostic des maladies, le développement pharmaceutique et les domaines liés à l'alimentation et à l'environnement. Parmi ces applications, en raison de sa performance de détection hautement sélective et hautement sensible, la LC/MS est un outil analytique essentiel pour la quantification des composants d'échantillons en traces.
Cependant, un problème intrinsèque se pose lors de l'utilisation de la LC/MS pour la quantification des composants en traces. Parce que la LC/MS est capable de détecter avec une haute sensibilité, les échantillons utilisés en LC/MS sont très faibles en concentration. Ces faibles concentrations d'échantillons entraînent une situation où l'adsorption des échantillons aux conteneurs et aux instruments peut être un facteur crucial pour réduire la fiabilité des résultats quantitatifs. Ceux qui sont impliqués dans la chimie analytique s'occupent de "rechercher comment obtenir des résultats analytiques hautement fiables à la fois simplement et rapidement", mais je me demande combien d'analystes considèrent ce problème d'adsorption aux conteneurs.
Il est clair pour la plupart que la LC/MS jouera un rôle important à l'avenir en tant que méthode quantitative hautement sensible. Par conséquent, augmenter la fiabilité des analyses quantitatives hautement sensibles effectuées à l'aide de la LC/MS est de la plus haute importance. Dans ce numéro, je me concentre sur l'adsorption des échantillons aux conteneurs, un problème souvent négligé par de nombreux analystes, en espérant contribuer à améliorer les analyses utilisant la LC/MS.
Écrire pour ce numéro m'a rappelé des souvenirs frustrants d'adsorption d'échantillons aux conteneurs. Il y a de cela 35 ans, la HPLC était utilisée pour analyser des formulations de peptides d'environ 20 résidus. Les systèmes HPLC de l'époque étaient loin des systèmes HPLC automatisés et sophistiqués disponibles aujourd'hui, utilisant une microsyringe (avec une surface interne en verre dépoli) pour obtenir un volume d'échantillon fixe (de plusieurs μg/mL) qui était injecté manuellement dans un injecteur. La variabilité entre les résultats était substantielle à l'époque, quel que soit le nombre de fois où l'analyse était répétée, et voir de tels résultats était alarmant. Pendant la phase d'essais et d'erreurs pour enquêter sur la cause de cette variabilité, j'ai remarqué que plus une microsyringe était rincée soigneusement, et plus longtemps un échantillon restait à l'intérieur de la seringue, plus les pics détectés étaient faibles.
J'ai finalement réalisé que la variabilité était causée par l'adsorption de l'échantillon à la microsyringe. Réalisant avec horreur l'effet important que l'adsorption seule avait sur la fiabilité de mes résultats, j'ai ressenti vivement le besoin de contrôler l'adsorption pendant le processus de manipulation de l'échantillon, de la préparation de l'échantillon à l'injection HPLC. Contrairement à la façon dont le phénomène d'adsorption est principalement négligé aujourd'hui avec les systèmes HPLC automatisés utilisés ces dernières années, de telles expériences amères ont augmenté ma compréhension de l'adsorption et sont devenues une motivation précieuse dans mon travail pour contrôler l'adsorption aux conteneurs et aux instruments. Ces expériences ont mis l'adsorption aux conteneurs et aux instruments au premier plan de mon esprit, et je m'efforce désormais toujours d'aborder la préparation des échantillons en comprenant d'abord le phénomène d'adsorption aux conteneurs et aux instruments.
J'ai récemment entendu un analyste LC/MS dire : "les pics des composants cibles dans les solutions d'échantillons de plasma sont détectés, mais aucun pic n'est détecté dans la solution standard" ou, "lorsque j'analyse une solution d'échantillon standard préparée la veille, aucun pic n'est détecté." Bien que la cause de ces problèmes puisse être attribuée à la dégradation basée sur la stabilité de l'échantillon, dans la majorité des cas, cela est facilement reconnu comme une adsorption au conteneur. En particulier avec les échantillons de plasma, nous savons que les impuretés dans l'échantillon s'adsorbent préférentiellement aux conteneurs, empêchant l'adsorption des composants cibles. C'est la même logique derrière l'utilisation de l'albumine de sérum bovin (BSA) comme agent de prévention de l'adsorption. En tout état de cause, tant que l'évaluation analytique par LC/MS continue de jouer un rôle important et de porter le poids de nos attentes, nous sommes appelés à tenter de comprendre à fond le phénomène d'adsorption des échantillons aux conteneurs afin d'obtenir des résultats hautement fiables.
Dans cette série d'expériences, j'ai interprété le mécanisme d'adsorption des échantillons aux conteneurs en termes du mécanisme de séparation HPLC. Le mécanisme de séparation pendant la HPLC consiste simplement à utiliser une phase mobile pour contrôler la force d'adsorption d'un soluté sur une phase stationnaire. Lorsque ce mécanisme est traduit au phénomène d'adsorption des échantillons aux conteneurs, la phase stationnaire devient le matériau du conteneur, la phase mobile devient la solution d'échantillon en cours de préparation, et le comportement de rétention des matériaux adsorbés sur les conteneurs est la force d'adsorption.
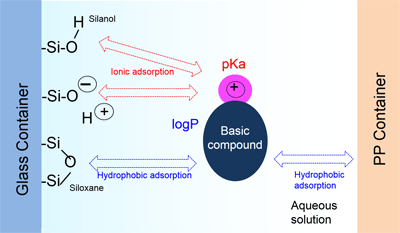
Fig. 1 Mécanisme d'Adsorption aux Fioles et Méthodes pour Inhiber l'Adsorption
Les conteneurs utilisés pour la préparation des échantillons sont normalement fabriqués dans l'un des deux matériaux principaux : des conteneurs en verre et des conteneurs en plastique (polypropylène : PP, polyéthylène : PE). La surface des conteneurs en verre est recouverte de groupes silanol hautement hydrophiles et de groupes siloxane hydrophobes (silanol déshydraté, qui apparaît lors de la fusion/formation de gel de silice à haute température). Par conséquent, dans une solution aqueuse, les conteneurs en verre suscitent simultanément l'adsorption ionique des molécules aux groupes silanol (mode d'échange d'ions positifs) et l'adsorption hydrophobe due aux groupes siloxane (phase inverse). Ce phénomène d'adsorption ionique est analogue au phénomène de traînée de pic et à l'augmentation de la rétention des composés basiques causés par les silanols résiduels dans une colonne HPLC. Pour les conteneurs en plastique, la seule adsorption causée par le matériau du conteneur (polymères de haut poids moléculaire) est l'adsorption hydrophobe. C'est-à-dire que le mécanisme d'adsorption diffère selon le matériau du conteneur. (Voir Fig. 1.) En raison de ces caractéristiques, les composés basiques avec un pKa élevé (constante de dissociation acide) ont tendance à s'adsorber au verre (silanol), et les composés avec un grand logP (coefficient de partage octanol/eau) ont tendance à s'adsorber à la fois aux conteneurs en verre et aux conteneurs en plastique. Pendant la préparation des échantillons, l'une des mesures prises pour prévenir l'adsorption est de d'abord sélectionner les conteneurs en fonction des propriétés physiques du composant cible (pKa et logP du composé).
En repensant à ces expériences frustrantes, puisque l'adsorption aux conteneurs est plus apparente avec des échantillons à faible concentration, trouver des conditions de préparation d'échantillons à faible concentration qui réduisent l'adsorption aux conteneurs et aux instruments est très important pour garantir la fiabilité des méthodes analytiques.
Ci-dessous, j'ai décrit ma méthode de préparation d'échantillons qui réduit l'adsorption aux conteneurs. La première chose à confirmer est de savoir si le ou les composés cibles sont basiques, acides ou neutres.
Ensuite, différentes méthodes de préparation d'échantillons doivent être utilisées en fonction de la préparation des échantillons dans des conteneurs en verre ou des conteneurs en PP.
1) Composés acides et composés neutres
Les composés acides et les composés neutres s'adsorbent principalement aux conteneurs en verre et en PP par adsorption hydrophobe. Par conséquent, un solvant organique (méthanol, acétonitrile, etc.) ou un tensioactif non ionique est ajouté à la solution d'échantillon pour réduire l'adsorption. Bien que dépendant du logP des composés cibles, l'ajout de 10 à 50 % de solvant organique ou d'environ 0,1 % de tensioactif est normalement efficace pour réduire l'adsorption pendant la préparation de l'échantillon.
2) Composés basiques
Il convient de faire attention lors du choix des matériaux de conteneurs pour la préparation des échantillons, car les composés basiques s'adsorbent aux conteneurs en verre et aux conteneurs en PP par des mécanismes différents. À titre d'exemple, un aperçu de la méthode utilisée pour réduire l'adsorption des composés basiques est montré dans la Fig. 2.
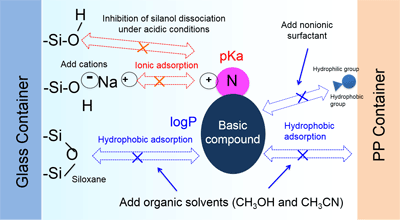
Fig.2 Mécanisme d'Adsorption aux Fioles et Méthodes pour Inhiber l'Adsorption
i) Conteneurs en verre
Les composés basiques s'adsorbent aux conteneurs en verre par adsorption ionique et adsorption hydrophobe simultanément, donc la préparation des échantillons doit être ajustée pour contrer les deux mécanismes d'adsorption. Du sel (NaCl, etc.) est ajouté pour placer des ions de sel positifs (Na+, etc.) en solution qui réduisent l'adsorption ionique en bloquant l'interaction avec les groupes silanol. Alternativement, la dissociation du silanol peut être empêchée en effectuant la préparation des échantillons dans des conditions acides (en ajoutant de l'acide phosphorique, de l'acide acétique, etc.). Comme pour les composés acides et neutres, l'adsorption hydrophobe est empêchée en ajoutant un solvant organique ou un tensioactif non ionique à la solution d'échantillon.
ii) Conteneurs en PP
Les conteneurs en PP donnent lieu à une adsorption hydrophobe, donc pour réduire cette adsorption, un solvant organique ou un tensioactif non ionique est ajouté à la solution d'échantillon.
Un moyen efficace de réduire l'adsorption dans les conteneurs en verre et en PP est donc d'avoir à la fois un sel et soit un solvant organique ou un tensioactif non ionique présents dans la solution d'échantillon.
Lors de la réalisation d'une analyse quantitative hautement sensible utilisant la HPLC ou la LC/MS, il faut également tenir compte de l'effet sur la séparation des ajustements d'échantillons effectués pour réduire l'adsorption, et de l'effet résultant sur la suppression des ions pendant la MS. De plus, les colonnes analytiques avec un diamètre de remplissage et des diamètres internes plus petits deviennent de plus en plus courantes car elles améliorent les performances de la HPLC et de la LC/MS, et ces changements doivent également être pris en compte en même temps que la quantité de solvant organique dans la solution d'échantillon (solution injectée) affecte la séparation. La réalité de l'analyse quantitative hautement sensible est que de nombreuses investigations sont nécessaires pour déterminer les conditions optimales de la solution d'échantillon pour réduire l'adsorption aux conteneurs.
Je me suis concentré sur le développement de fioles polyvalentes à faible adsorption adaptées à une utilisation dans les auto-échantillonneurs HPLC, où la finition de surface du conteneur est optimisée pour réduire l'adsorption ionique et hydrophobe des échantillons.
Dans le prochain numéro de ce journal, je discuterai de la manière dont les fioles spécialement développées réduisent l'adsorption, en utilisant les peptides et les composés basiques comme exemples spécifiques de composés.
>>L'Horreur de l'Adsorption des Échantillons aux Conteneurs Partie 2
>>L'Horreur de l'Adsorption des Échantillons aux Conteneurs Partie 3
Pour plus de détails, visitez







