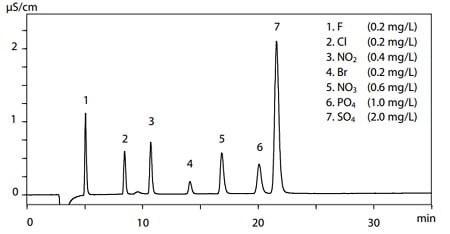
Fig. 2 Chromatogramme de la solution standard d'anions
Tableau 1. Groupes fonctionnels typiques utilisés dans la phase stationnaire d'échange d'ions
| Force ionique | Groupes fonctionnels typiques | |
|---|---|---|
| Chromatographie par échange de cations | Forte (SCX) | Acide sulfonique |
| Faible (WCX) | Acide carboxylique | |
| Chromatographie par échange d'anions | Forte (SAX) | Ammonium quaternaire |
| Faible (WAX) | Amine tertiaire |
La Fig.1 montre le fonctionnement de la chromatographie par échange d'anions.
Dans la phase stationnaire de la chromatographie par échange d'anions, on utilise des matériaux de remplissage modifiés avec des groupes d'échange d'ions chargés positivement. Lorsque la phase mobile (éluant) entre dans la colonne, elle est absorbée sur les groupes d'échange d'ions de la phase stationnaire en raison de l'attraction électrostatique. La phase mobile introduit continuellement des anions dans la colonne, entraînant une adsorption et une désorption répétées des anions entre les phases stationnaire et mobile, c'est-à-dire un état d'équilibre. Lorsqu'un échantillon contenant des anions est introduit dans la colonne pendant cet état, les anions de l'échantillon sont adsorbés par des interactions électrostatiques avec les groupes fonctionnels de la phase stationnaire. En même temps, les anions de la phase mobile qui étaient auparavant adsorbés sur la phase stationnaire sont désorbés. Les anions de l'échantillon adsorbés sur la phase stationnaire sont ensuite désorbés et adsorbés sur le groupe d'échange d'ions suivant. Ce phénomène se répète jusqu'à ce que les anions de l'échantillon traversent complètement la colonne et soient élués.
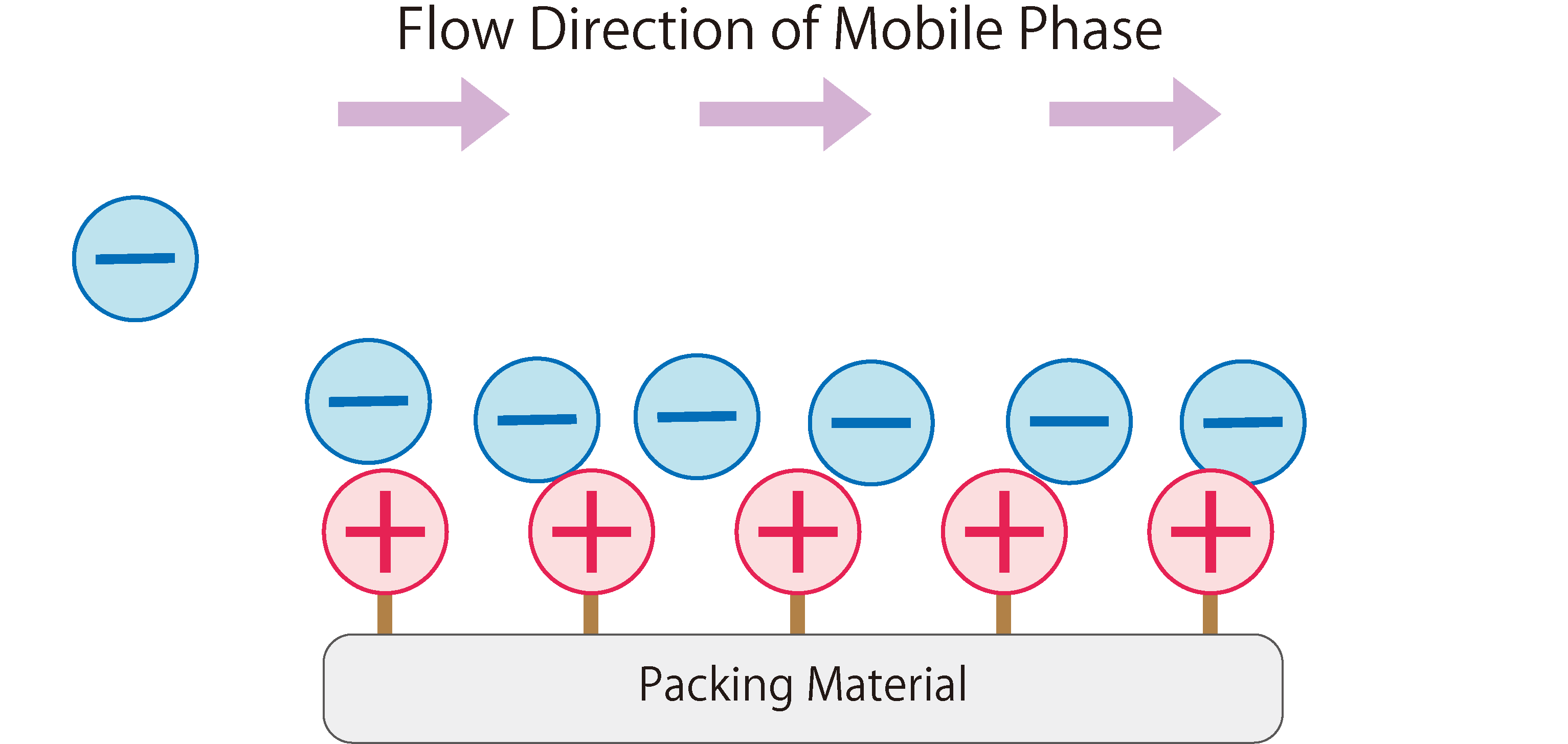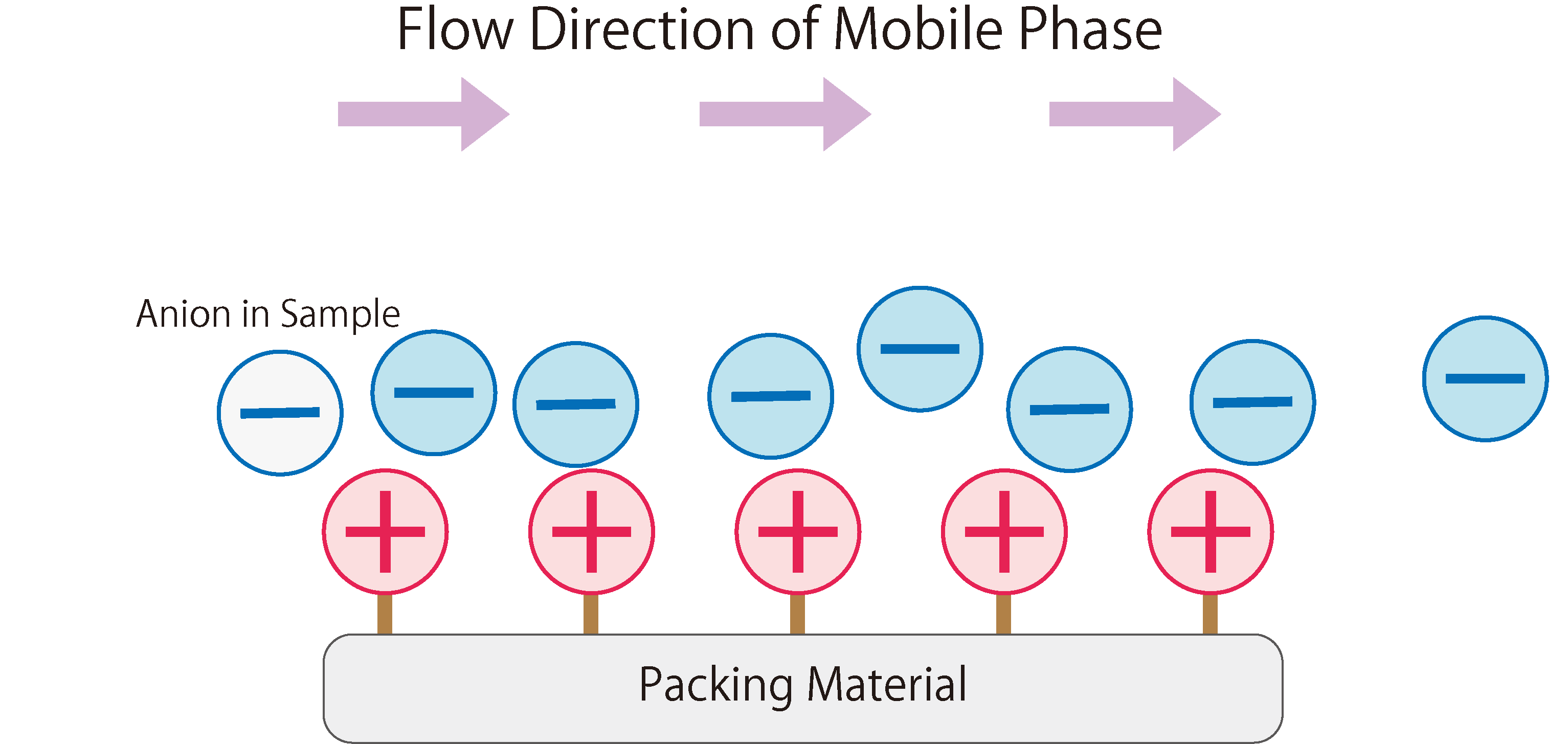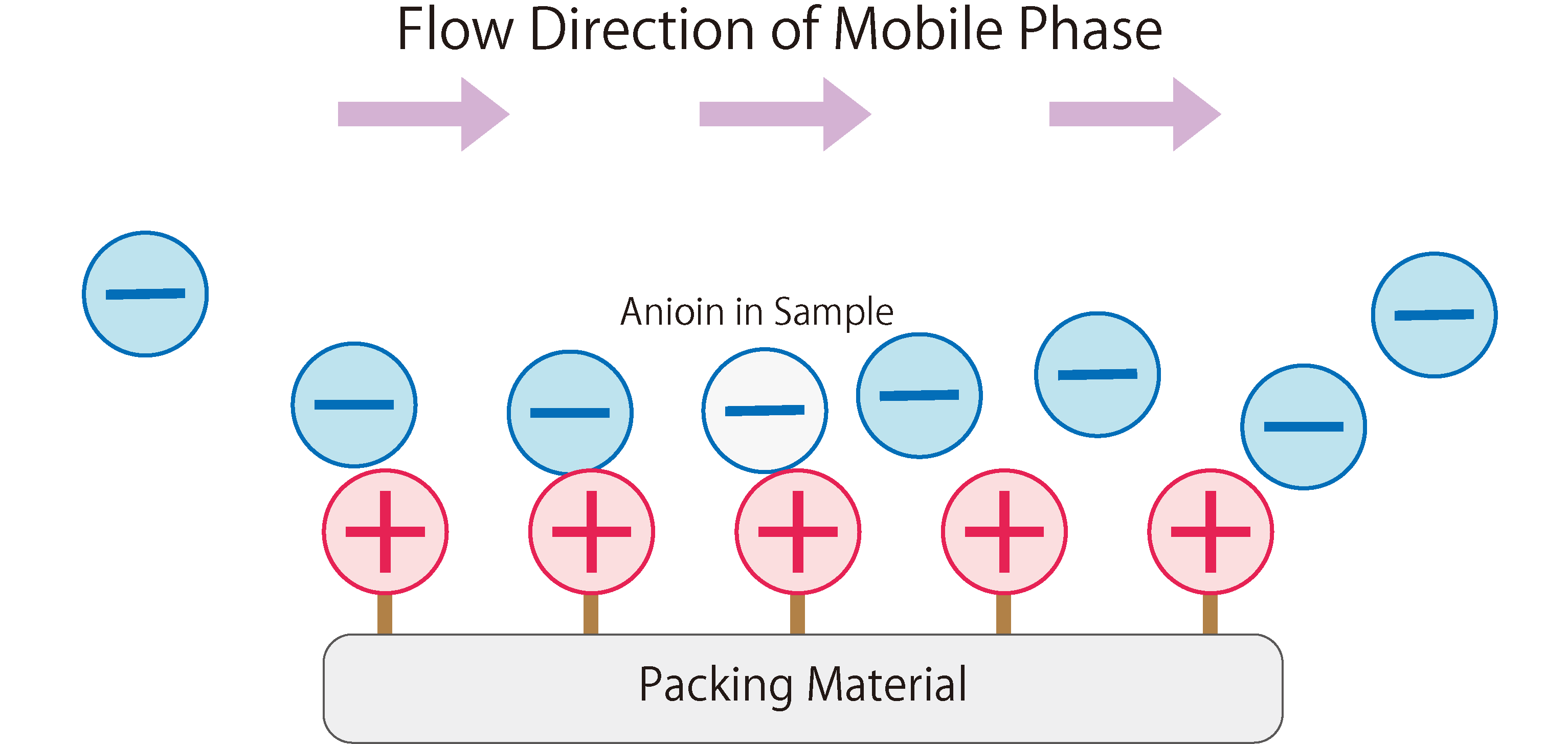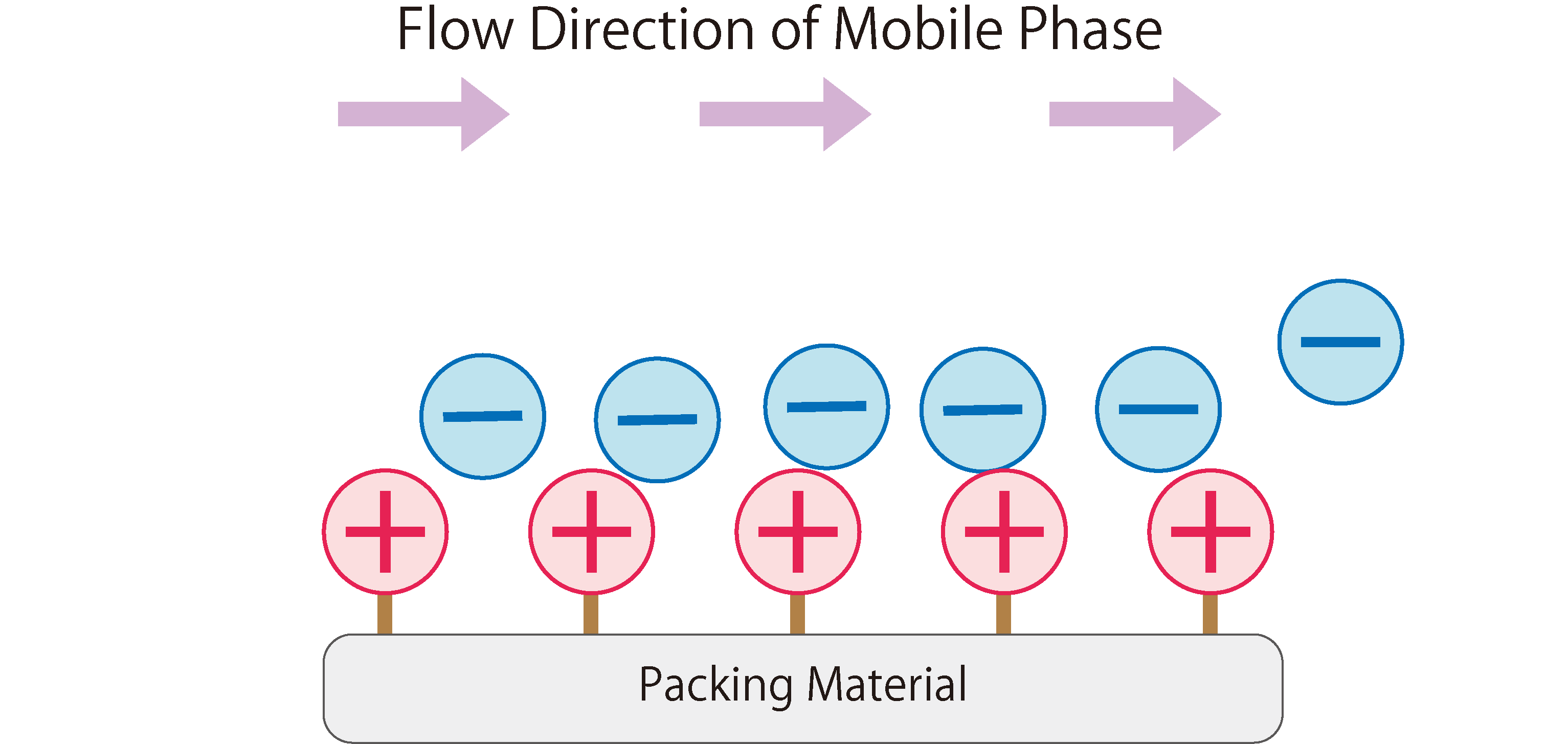
Fig. 1 Le fonctionnement de la chromatographie par échange d'anions
Les différents types d'ions dans l'échantillon interagissent différemment avec les groupes d'échange d'ions, ce qui entraîne des différences dans la vitesse à laquelle ils se déplacent à travers la colonne. Cette différence est utilisée pour séparer les ions dans l'échantillon. Les ions avec une valence plus petite interagissent moins avec les groupes d'échange d'ions et sont donc élués plus rapidement de la colonne. Cependant, les ions avec la même valence ou des éléments homologues seront toujours élués plus rapidement s'ils ont des rayons ioniques plus petits.

Fig. 2 Chromatogramme de la solution standard d'anions
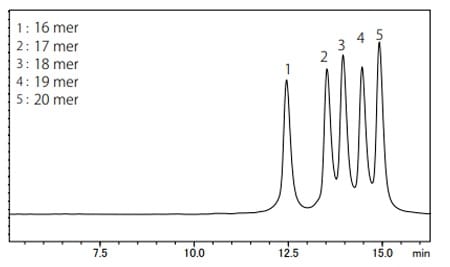
Fig. 3 Chromatogramme du mélange d'oligonucléotides
La Fig.2 montre le chromatogramme des solutions standards pour sept anions. Une colonne de chromatographie par échange d'anions (Shim-pack IC-SA3) a été utilisée dans ce cas d'analyse. Il a été montré que F, Cl et Br dans la solution standard de mélange d'anions étaient des éléments halogènes, et qu'ils étaient élués dans l'ordre du plus petit au plus grand rayon ionique, bien que leurs valeurs ioniques soient les mêmes.
La Fig.3 montre le chromatogramme d'un mélange de cinq séquences d'oligonucléotides. Une colonne de chromatographie par échange d'anions (Shim-pack BIO IEX Q-NP) a été utilisée dans ce cas d'analyse des oligonucléotides. La séparation des oligonucléotides est basée sur le nombre de groupes phosphate dans l'oligonucléotide, c'est-à-dire la différence de charges négatives. Par conséquent, chaque oligonucléotide a été séparé par leur longueur.
En chromatographie par échange d'ions, si un échantillon contient des composés dont l'état ionique change avec le pH, changer le pH de la phase mobile ainsi que la concentration en sel de la phase mobile peut modifier l'ordre d'élution.
En savoir plus
Lien
Produits connexes
Le HIC-ESP est un nouveau chromatographe à suppression d'anions avec suppresseur électrodialytique intégré, offrant le même faible report et la même excellente précision d'injection caractéristique des HPLC de Shimadzu pour vous apporter des résultats hautement fiables.
La chromatographie ionique (IC) est utilisée pour l'analyse des ions inorganiques et organiques. Elle est catégorisée en IC avec suppresseur et IC sans suppresseur. L'IC sans suppresseur est composée d'un système HPLC conventionnel combiné à un détecteur de conductivité, tandis que l'IC avec suppresseur nécessite un suppresseur supplémentaire.
Les colonnes Shim-pack Bio IEX sont disponibles en chimies Q (ammonium quaternaire) et SP (sulfopropyle) et sont basées sur des polymères hydrophiles poreux (colonnes Q et SP) et non poreux (colonnes Q-NP et SP-NP) avec une faible adsorption non spécifique.