2-1) Augmentation de la température de la solution
Dans des situations telles que lorsqu'un solvant froid provenant du stockage est utilisé dans une pièce chaude, la solubilité saturée des gaz diminue progressivement à mesure que la température augmente, ce qui entraîne la formation de bulles de gaz dissous en excès. C'est le même principe qui provoque la formation plus vigoureuse de gaz carbonique (CO2) lorsque les boissons gazeuses sont réchauffées avant ouverture.
La figure 2 montre les courbes de solubilité saturée pour O2 et N2 par rapport à l'eau, étant donné une pression partielle d'une atmosphère pour les gaz. Étant donné que l'air contient 20 % O2 et 78 % N2, si exposé à l'air, la quantité d'O2 et de N2 dissous est d'environ 0,2 ou 0,8 fois le niveau indiqué, respectivement.
Remarque : 1 atmosphère (1 atm) = 1,013 × 105 Pa
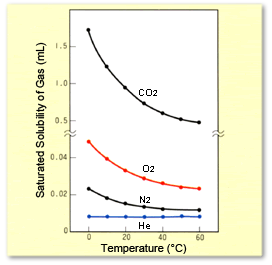
Effets de la température sur la quantité de CO2, O2, N2 et He dissous (à des pressions partielles de 1 atm).






