Méthodes analytiques pour les acides organiques
En tant que composant clé qui détermine l'"umami" (saveur ou goût) dans les aliments, les acides organiques rivalisent avec les acides aminés et les sucres en tant que l'une des substances les plus couramment analysées. Cette page discute des méthodes d'analyse des acides organiques utilisant la HPLC.
Méthodes de Séparation
Les trois principaux modes de séparation des acides organiques sont l'échange d'anions, l'exclusion des ions et la phase inverse. Les caractéristiques de chacun de ces modes sont brièvement décrites ci-dessous.
Mode d'Échange d'Ions
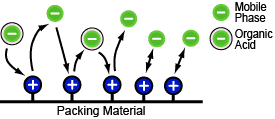
Mode d'Échange d'Ions
Ce mode de séparation peut être considéré comme les ions négatifs de la phase mobile et les ions acides organiques (ions négatifs) en compétition pour les ions positifs dans le matériau de garnissage. Le comportement de rétention de la colonne varie en fonction du rayon et de la valence des ions acides organiques. De nombreux acides organiques nécessitent l'utilisation d'une élution en gradient pour la séparation, ce qui augmente également le temps d'analyse.
Mode d'Exclusion d'Ions
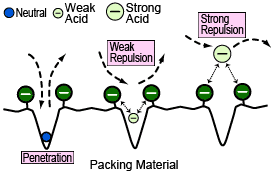
Mode d'Exclusion d'Ions
C'est le mode le plus couramment utilisé pour l'analyse des acides organiques. Il utilise un polymère échangeur de cations de type H (hydrogène) pour le matériau de garnissage et les acides organiques sont séparés par la différence de tailles d'exclusion de Donnan entre la phase stationnaire (avec des groupes échangeurs d'ions de type H) et la phase mobile.
Dans ce mode, les acides forts sont soumis à une forte exclusion électrostatique causée par la charge négative de la phase stationnaire, ce qui les empêche de pénétrer dans les pores du matériau de garnissage. Pendant ce temps, pour les acides faibles, tels que les acides organiques, le degré auquel ils peuvent pénétrer dans les pores est déterminé par la taille de la charge (considérez-le comme le pKa), ce qui entraîne des différences dans le temps d'élution (séparation). Dans l'exemple montré ci-dessous à droite, les acides avec de grandes charges négatives (petit pKa), tels que les acides citrique et lactique, sont soumis à un effet d'exclusion électrostatique plus important que les acides tels que l'acide acétique et, par conséquent, sont éludés plus rapidement. Par conséquent, en principe, les acides organiques éludent dans l'ordre de la taille du pKa, en commençant par les valeurs de pKa les plus basses, et terminent leur élution avant que les substances neutres ne commencent à éluer (position pour les éléments qui ont complètement pénétré les pores).
Cependant, en réalité, une interaction hydrophobe se produit également avec une partie du substrat de garnissage (styrène-divinylbenzène), ce qui peut retarder l'élution des acides organiques hydrophobes en particulier. Par exemple, l'acide valérique élue beaucoup plus tard que l'acide acétique bien qu'il y ait peu de différence dans leurs valeurs de pKa. Cela est dû au fait que l'acide valérique est retenu plus fortement en raison d'une interaction hydrophobe avec le matériau du substrat.
De cette manière, une combinaison de trois facteurs - exclusion électrostatique due à la phase stationnaire chargée négativement, interaction hydrophobe avec la matrice de la phase stationnaire et pénétration dans les pores de la phase stationnaire, détermine les temps d'élution. Ce mode est largement utilisé car c'est une méthode simple qui nécessite un ajustement minimal des paramètres de la phase mobile.
Mode Phase Inverse
Ce mode offre la plus large applicabilité pour la HPLC, mais il n'est pas très largement utilisé pour analyser les acides organiques. Cela est dû au fait que les acides organiques sont hydrophiles, ce qui peut souvent empêcher une rétention ou une sélectivité adéquates. Cependant, des colonnes en phase inverse commerciales qui peuvent retenir suffisamment même les substances hautement hydrophiles sont récemment devenues disponibles sur le marché.
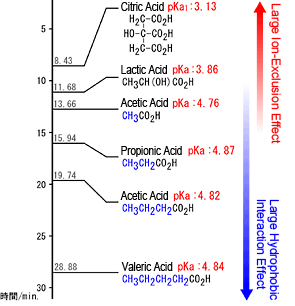
Exemple de Valeurs de pKa et Temps d'Élution des Acides Organiques
Note : Les valeurs de pKa ont été obtenues à partir de Seikagaku Deta Bukku (Manuel de Biochimie) (1979) et Kagaku Binran Kiso-Hen (Manuel de Chimie Générale), 2e éd. (1975). Une comparaison de diverses références a indiqué une différence allant jusqu'à 0,3, mais ces valeurs étaient proches de celles des références datées depuis 2000, telles que le Merck Index, les ressources académiques sur la chimie aux États-Unis, les dictionnaires chimiques et les dictionnaires biochimiques. Par conséquent, ces anciennes références avec des données documentées respectives ont été utilisées.
Méthodes de Détection
La méthode de détection la plus simple, la détection UV directe, détecte l'absorption du groupe carboxyle dans la plage de 200 à 210 nm. Cependant, il existe de nombreuses substances organiques avec une absorption dans cette plage de longueurs d'onde, ce qui peut entraîner une interférence significative des contaminants et rendre difficile la quantification précise des composants à moins que l'échantillon ne soit très pur. Les détecteurs d'indice de réfraction peuvent également être utilisés, mais en plus d'une sélectivité plus faible, ils ont également un problème de sensibilité. La détection directe en utilisant un détecteur de conductivité électrochimique est une autre méthode, mais elle nécessite de réduire la conductivité électrochimique de fond de la phase mobile.
Les méthodes de détection post-colonne qui peuvent détecter sélectivement les acides organiques avec une haute sensibilité incluent l'indicateur de pH - détection par absorption visible et le tampon de pH - détection par conductivité électrochimique. La méthode de l'indicateur de pH utilise un changement de couleur de l'indicateur de pH pour détecter les acides organiques, mais elle présente des problèmes de linéarité et de facilité d'utilisation. En revanche, la méthode de tampon de pH offre une excellente sensibilité, sélectivité et précision.
Méthode de Tampon de pH
Typiquement, une phase mobile acide est utilisée dans le mode d'exclusion des ions, qui est largement utilisé pour l'analyse des acides organiques. Cela signifie que la dissociation est inhibée pour les acides faibles tels que les acides organiques. De plus, comme la conductivité électrochimique de fond est élevée, l'utilisation d'un détecteur de conductivité électrochimique dans ces conditions ne fournira pas une sensibilité adéquate. Par conséquent, dans cette méthode de tampon de pH, un tampon de pH est continuellement ajouté à l'effluent de la colonne pour ajuster le pH à un niveau proche de la neutralité pour promouvoir la dissociation des acides organiques et réduire le bruit de fond. L'effluent est ensuite dirigé vers un détecteur de conductivité électrochimique qui peut détecter les acides organiques avec une haute sensibilité et sélectivité.
La figure à droite montre un exemple de la relation entre le pH de l'éluant et le niveau de dissociation pour l'acide acétique. Au niveau de pH à l'intérieur de la colonne (environ 3), il n'y a presque pas de dissociation de l'acide acétique. Cela entraîne une exclusion ionique faible dans la colonne, ce qui permet une bonne séparation des autres acides organiques. En revanche, le pH est neutre à l'entrée du détecteur, donc presque tout l'acide acétique est dissocié. Cela montre que promouvoir la dissociation en utilisant un réactif tampon de pH de cette manière permet une détection avec une haute sensibilité.
En d'autres termes, cette méthode "fait d'une pierre deux coups" en réduisant le niveau de fond de la phase mobile, tout en augmentant la sensibilité en favorisant la dissociation de l'acide organique.
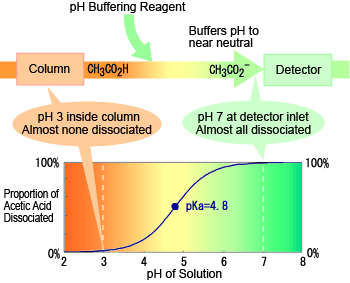
État de l'Acide Organique dans la Méthode de Tampon de pH Presque aucune dissociation pendant la séparation dans la colonne, mais presque complètement dissocié lors de la détection
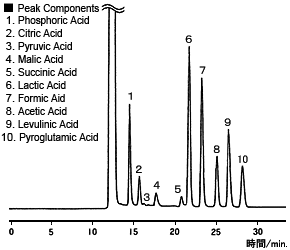
Chromatogramme de la Sauce Soja
La méthode de tampon de pH permet non seulement de détecter les acides organiques avec une bonne sensibilité et sélectivité, mais elle fournit également des courbes d'étalonnage avec une large plage linéaire. Par conséquent, elle est efficace pour analyser une large gamme de concentrations d'échantillons. Par conséquent, elle est utilisée dans le Système d'Analyse des Acides Organiques de Shimadzu.
L'exemple à droite provient de l'analyse de la sauce soja. L'utilisation de ce système permet d'analyser les acides organiques avec une bonne précision, mais sans interférence des contaminants, même pour des échantillons tels que la sauce soja. (Yt, Wk)






